本报讯 6 月 8 日,中国科大周荣斌/江维教授团队在 Immunity 发表研究论文,率先证明 ILC3s 可直接识别组织损伤并发现GPR34 在 其 中 发 挥 关 键作用。
免疫识别是免疫学研究的核心科学问题。固有免疫识别受体能够识别病原微生物感染以及机体组织损伤或者内环境失衡产生 的 内 源 性 “ 危 险 信号”,从而快速启动固有免疫和炎症反应,因而在免疫防御、免疫稳态和炎症性疾病发生中发挥关键作用。近年来病原微生物的固有免疫识别机制研究取得了极大的进展,目前已经发现超过50种固有免疫识别受体。
三 型 固 有 淋 巴 细 胞(type3innatelymphoidcells, ILC3s)是近年发现的固有免疫细胞,主要位于粘膜组织。ILC3s 可通过产生 IL-22 促进上皮细胞增 殖 和 修 复 , 因 而 在 肠道、皮肤等粘膜组织稳态维持方面发挥关键作用。
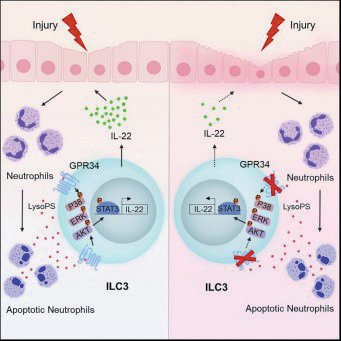
利 用 葡 聚 糖 硫 酸 钠(dextransodiumsulfate,DSS) 诱 导 的 结 肠 损 伤 模型,研究者发现清除中性粒细胞会导致小鼠肠道损伤加重、修复减弱。机制研究发现清除中性粒细胞后小鼠结肠组织中 ILC3s细胞的活化及产生的 IL-22 减弱,且补充 IL-22 可恢 复 DSS 诱 导 的 结 肠 损伤,说明结肠损伤过程中中性粒细胞介导了 ILC3s的活化。为进一步探究中性粒细胞如何活化 ILC3s,利用体外共培养和代谢组学分析,研究者发现凋亡的中性粒细胞可通过释放溶 血 磷 脂 酰 丝 氨 酸 诱 导ILC3s 活化和 IL-22 产生。进一步利用基因缺陷小鼠和小分子拮抗剂,研究者利用 Gpr34 全身敲除小鼠和 ILC3s 条件敲除小鼠证明GPR34在结肠和皮肤损伤 模 型 中 对 ILC3s 活 化 、IL-22 产生及组织修复中均发挥重要作用 (如图)。该项研究得到了审稿人的高度评价,认为该项工作“首次证明 ILC3s可感应危险信号”“发现了一种新的ILC3s活化方式”。
该研究的创新性体现在以下三个方面:首次证明三型固有淋巴细胞可直接识别组织损伤;发现GPR34是一种新的危险识别受体;提示GPR34可作为治疗炎症性肠病和皮肤炎症的潜在干预靶标。
我校博士后王夏琼、博士研究生蔡娟、林柏龙为论文共同第一作者。
( 生 命 科 学 与 医 学 部 基 础 医 学院、附属第一医院 中科院天然免疫与慢性疾病重点实验室 合肥微尺度物质科学研究中心 科研部)
